No products in the cart.
Công nghệ UV
Quang phổ UV-Vis là gì?
Quang phổ tia cực tím (UV-Vis) là một kỹ thuật được sử dụng rộng rãi trong nhiều lĩnh vực khoa học, từ nuôi cấy vi khuẩn , xác định thuốc, kiểm tra và định lượng độ tinh khiết axit nucleic, đến kiểm tra chất lượng trong ngành công nghiệp đồ uống và nghiên cứu hóa học. Bài viết này sẽ mô tả cách thức hoạt động của quang phổ UV-Vis, cách phân tích dữ liệu đầu ra, các điểm mạnh và hạn chế của kỹ thuật cũng như một số ứng dụng của nó, giúp bạn đọc hiểu rõ hơn về quang phổ UV-Vis.
Quang phổ UV-Vis là gì?
Quang phổ UV-Vis là một kỹ thuật phân tích đo lượng bước sóng rời rạc của tia UV hoặc ánh sáng khả kiến được hấp thụ hoặc truyền qua mẫu so với mẫu chuẩn hoặc mẫu trắng. Tính chất này bị ảnh hưởng bởi thành phần mẫu, có khả năng cung cấp thông tin về những gì có trong mẫu và ở nồng độ nào. Vì kỹ thuật quang phổ này dựa vào việc sử dụng ánh sáng, trước tiên chúng ta hãy xem xét các đặc tính của ánh sáng.
Ánh sáng có một lượng năng lượng tỉ lệ nghịch với bước sóng của nó. Như vậy, ánh sáng có bước sóng ngắn hơn mang nhiều năng lượng hơn và bước sóng dài hơn mang ít năng lượng hơn. Một lượng năng lượng cụ thể là cần thiết để thúc đẩy các điện tử trong một chất lên trạng thái năng lượng cao hơn mà chúng ta có thể phát hiện ra là sự hấp thụ. Các electron trong các môi trường liên kết khác nhau trong một chất đòi hỏi một lượng năng lượng cụ thể khác nhau để thúc đẩy electron lên trạng thái năng lượng cao hơn. Đây là lý do tại sao sự hấp thụ ánh sáng xảy ra đối với các bước sóng khác nhau trong các chất khác nhau. Con người có thể nhìn thấy quang phổ ánh sáng khả kiến, từ khoảng 380 nm, mà chúng ta thấy là màu tím, đến 780 nm, mà chúng ta thấy là màu đỏ. 1Ánh sáng UV có bước sóng ngắn hơn bước sóng của ánh sáng nhìn thấy đến khoảng 100 nm. Do đó, ánh sáng có thể được mô tả bằng bước sóng của nó, có thể hữu ích trong quang phổ UV-Vis để phân tích hoặc xác định các chất khác nhau bằng cách định vị các bước sóng cụ thể tương ứng với độ hấp thụ cực đại (xem phần Ứng dụng của quang phổ UV-Vis).
Máy quang phổ UV-Vis hoạt động như thế nào?
Mặc dù có nhiều biến thể trên máy quang phổ UV-Vis, để hiểu rõ hơn về cách hoạt động của máy quang phổ UV-Vis, chúng ta hãy xem xét các thành phần chính, được mô tả trong Hình 1.
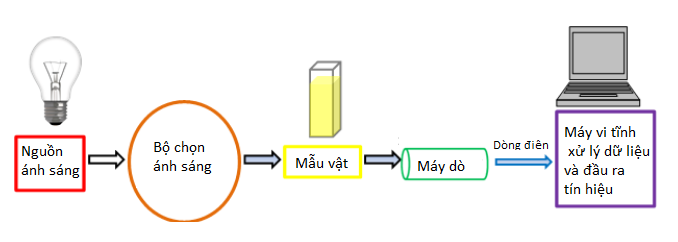 Hình 1: Sơ đồ đơn giản của các thành phần chính trong máy quang phổ UV-Vis. Nhà cung cấp hình ảnh: Tiến sĩ Justin Tom.
Hình 1: Sơ đồ đơn giản của các thành phần chính trong máy quang phổ UV-Vis. Nhà cung cấp hình ảnh: Tiến sĩ Justin Tom.
Nguồn sáng
Là một kỹ thuật dựa trên ánh sáng, một nguồn ổn định có thể phát ra ánh sáng trên nhiều bước sóng là điều cần thiết. Một đèn xenon thường được sử dụng làm nguồn sáng cường độ cao cho cả dải UV và dải nhìn thấy được. Tuy nhiên, đèn xenon có giá thành cao hơn và kém ổn định hơn so với đèn vonfram và đèn halogen.
Đối với các dụng cụ sử dụng 2 đèn, một đèn vonfram hoặc halogen thường được sử dụng cho ánh sáng nhìn thấy, trong khi đèn đơteri là nguồn phổ biến của tia UV. Vì cần hai nguồn sáng khác nhau để quét cả tia UV và bước sóng nhìn thấy, nên nguồn sáng trong thiết bị phải chuyển đổi trong quá trình đo. Trong thực tế, sự chuyển đổi này thường xảy ra trong quá trình quét từ 300 đến 350 nm nơi phát xạ ánh sáng tương tự nhau từ cả hai nguồn sáng và quá trình chuyển đổi có thể được thực hiện suôn sẻ hơn.
Lựa chọn bước sóng
Trong bước tiếp theo, các bước sóng ánh sáng nhất định phù hợp với loại mẫu và chất phân tích để phát hiện phải được chọn để kiểm tra mẫu từ các bước sóng rộng do nguồn sáng phát ra. Các phương pháp hiện có cho việc này bao gồm:
- Máy đơn sắc: Máy đơn sắc tách ánh sáng thành một dải hẹp có bước sóng. Người ta thường dựa vào cách tử nhiễu xạ có thể xoay để chọn góc tới và góc phản xạ để chọn bước sóng ánh sáng mong muốn. Tần số rãnh của cách tử nhiễu xạ thường được đo bằng số rãnh trên mm. Tần số rãnh cao hơn cung cấp độ phân giải quang học tốt hơn nhưng dải bước sóng có thể sử dụng hẹp hơn. Tần số rãnh thấp hơn cung cấp dải bước sóng có thể sử dụng lớn hơn nhưng độ phân giải quang học kém hơn. 300 đến 2000 rãnh trên mm có thể được sử dụng cho mục đích quang phổ UV-Vis nhưng tối thiểu là 1200 rãnh trên mm là điển hình. Chất lượng của các phép đo quang phổ nhạy cảm với các khuyết tật vật lý trong cách tử nhiễu xạ và trong thiết lập quang học. Do đó, các cách tử nhiễu xạ được kiểm soát có xu hướng có nhiều khuyết tật hơn các cách tử nhiễu xạ ba chiều được phát sáng. Cách tử nhiễu xạ ba chiều được làm mờ có xu hướng cung cấp các phép đo chất lượng tốt hơn đáng kể.
- Bộ lọc hấp thụ: Bộ lọc hấp thụ thường được làm bằng thủy tinh màu hoặc nhựa được thiết kế để hấp thụ các bước sóng ánh sáng cụ thể.
- Bộ lọc giao thoa: Còn được gọi là bộ lọc lưỡng sắc, các bộ lọc thường được sử dụng này được làm bằng nhiều lớp vật liệu điện môi, nơi xảy ra sự giao thoa giữa các lớp vật liệu mỏng. Các bộ lọc này có thể được sử dụng để loại bỏ các bước sóng không mong muốn bằng cách can thiệp triệt tiêu, do đó hoạt động như một bộ chọn bước sóng.
- Bộ lọc ngắt: Bộ lọc ngắt cho phép ánh sáng ở dưới (đường tắt) hoặc ở trên (đường dài) một bước sóng nhất định đi qua. Chúng thường được thực hiện bằng cách sử dụng các bộ lọc nhiễu.
- Bộ lọc thông dải: Bộ lọc thông dải cho phép một loạt các bước sóng đi qua có thể được thực hiện bằng cách kết hợp các bộ lọc thông ngắn và thông dài với nhau.
Bộ khuếch đại đơn sắc được sử dụng phổ biến nhất cho quá trình này do tính linh hoạt của chúng. Tuy nhiên, các bộ lọc thường được sử dụng cùng với các bộ đơn sắc để thu hẹp các bước sóng ánh sáng được chọn hơn nữa để có các phép đo chính xác hơn và cải thiện tỷ lệ tín hiệu trên nhiễu.
Phân tích mẫu
Cho dù bộ chọn bước sóng nào được sử dụng trong máy quang phổ, ánh sáng sau đó sẽ truyền qua một mẫu. Đối với tất cả các phép phân tích, việc đo mẫu chuẩn, thường được gọi là “mẫu trắng”, chẳng hạn như cuvet chứa đầy dung môi tương tự được sử dụng để chuẩn bị mẫu, là bắt buộc. Nếu dung dịch đệm trong nước có chứa mẫu được sử dụng để đo thì dung dịch đệm trong nước không chứa chất cần quan tâm được sử dụng làm chuẩn. Khi kiểm tra môi trường nuôi cấy vi khuẩn, môi trường nuôi cấy vô trùng sẽ được sử dụng làm chất tham khảo. Sau đó, tín hiệu mẫu chuẩn được thiết bị sử dụng tự động để giúp thu được các giá trị độ hấp thụ thực của chất phân tích.
Điều quan trọng là phải biết các vật liệu và điều kiện được sử dụng trong các thí nghiệm quang phổ UV ‑ Vis. Ví dụ, phần lớn cuvet bằng nhựa không thích hợp cho các nghiên cứu hấp thụ tia cực tím vì nhựa thường hấp thụ tia cực tím. Kính có thể hoạt động như một bộ lọc, thường hấp thụ phần lớn UVC (100‑280 nm) và UVB (280‑315 nm) nhưng cho phép một số tia UVA (315‑400 nm) để đi qua. Do đó, người giữ mẫu thạch anh được yêu cầu để kiểm tra tia cực tím vì thạch anh trong suốt đối với phần lớn ánh sáng tia cực tím. Không khí cũng có thể được coi như một bộ lọc vì ánh sáng có bước sóng ngắn hơn khoảng 200 nm được hấp thụ bởi oxy phân tử trong không khí. Cần có một thiết lập đặc biệt và đắt tiền hơn đối với các phép đo có bước sóng ngắn hơn 200 nm, thường liên quan đến hệ thống quang học chứa đầy khí argon tinh khiết. Các hệ thống không có cuvet cũng có sẵn cho phép phân tích các thể tích mẫu rất nhỏ, ví dụ như trong phân tích DNA hoặc RNA.
Phát hiện
Sau khi ánh sáng đi qua mẫu, một máy dò được sử dụng để chuyển đổi ánh sáng thành tín hiệu điện tử có thể đọc được. Nói chung, máy dò dựa trên lớp phủ quang điện hoặc chất bán dẫn.
Một lớp phủ quang điện đẩy ra các êlectron mang điện tích âm khi bị ánh sáng chiếu vào. Khi êlectron bị đẩy ra, một dòng điện tỉ lệ với cường độ ánh sáng được tạo ra. Ống nhân quang (PMT) là một trong những thiết bị phát hiện phổ biến hơn được sử dụng trong quang phổ UV ‑ Vis. PMT dựa trên hiệu ứng quang điện để ban đầu đẩy các electron ra khi tiếp xúc với ánh sáng, sau đó là sự nhân liên tiếp các electron bị đẩy ra để tạo ra dòng điện lớn hơn đầu dò PMT đặc biệt hữu ích để phát hiện mức độ ánh sáng rất thấp.
Khi chất bán dẫn tiếp xúc với ánh sáng thì có dòng điện tỉ lệ với cường độ ánh sáng chạy qua. Cụ thể hơn, điốt quang và thiết bị ghép nối tích điện (CCD) là hai trong số những bộ dò phổ biến nhất dựa trên công nghệ bán dẫn.Sau khi dòng điện được tạo ra từ bất kỳ máy dò nào được sử dụng, tín hiệu sau đó sẽ được nhận dạng và xuất ra máy tính hoặc màn hình. Hình 2 và 3 cho thấy một số sơ đồ ví dụ đơn giản về cách bố trí máy quang phổ UV-Vis.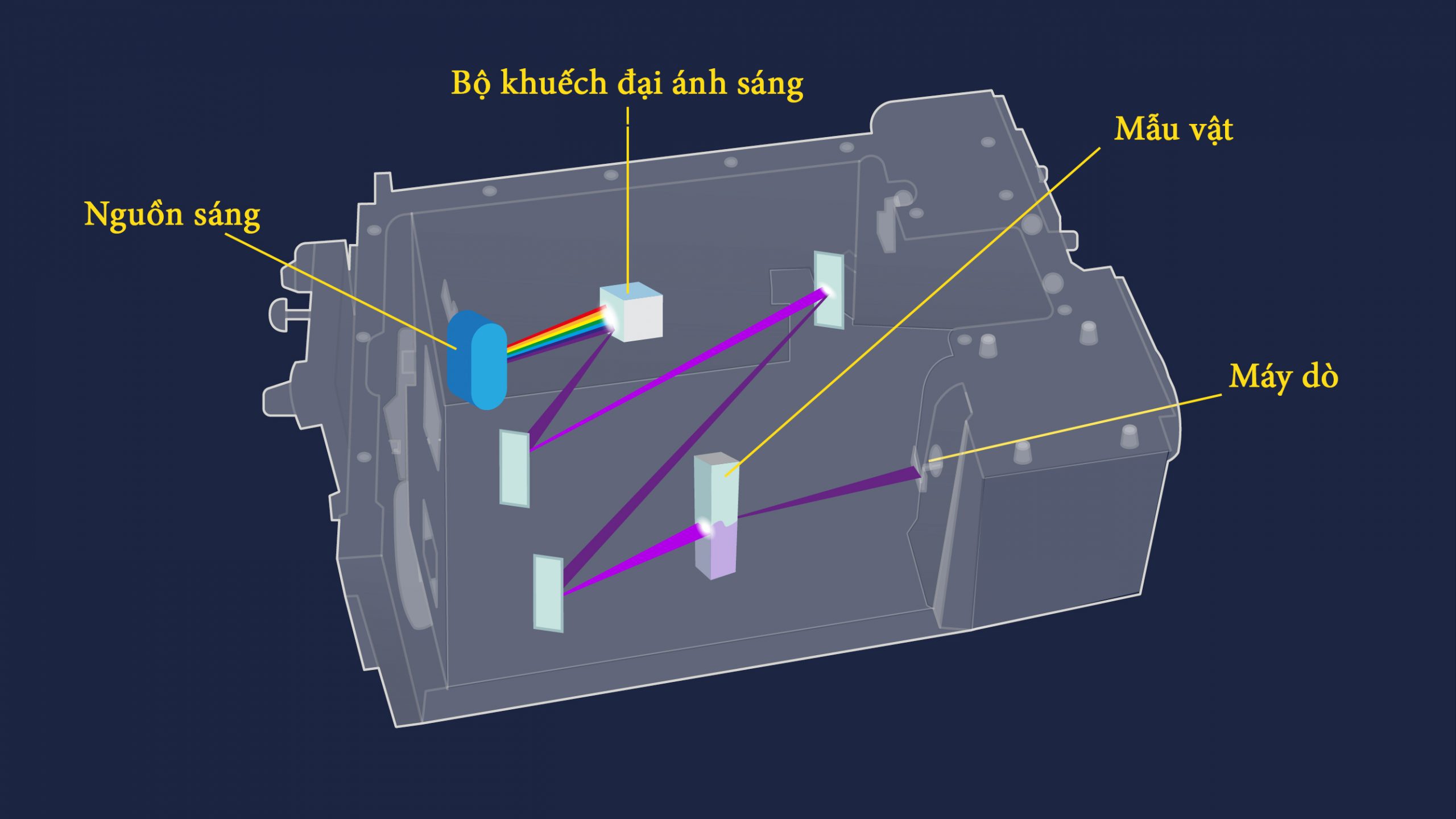 Hình 2: Sơ đồ hệ thống quang phổ UV-Vis dựa trên cuvet
Hình 2: Sơ đồ hệ thống quang phổ UV-Vis dựa trên cuvet
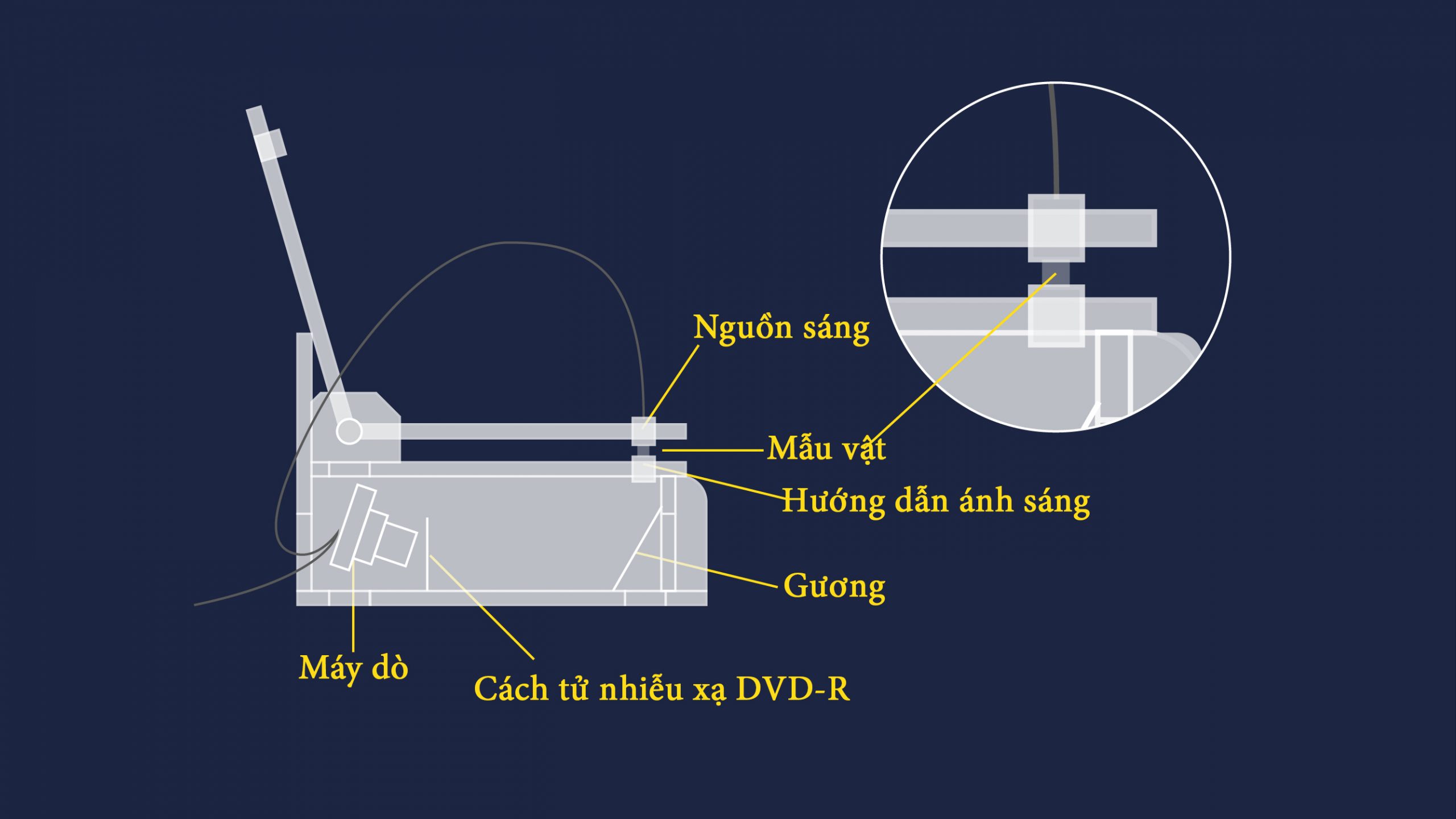
Hình 3: Sơ đồ của một hệ thống quang phổ UV-Vis không có cuvet
Phân tích quang phổ UV-Vis, phổ hấp thụ và đơn vị độ hấp thụ
Thông tin về quang phổ UV-Vis có thể được trình bày dưới dạng đồ thị của độ hấp thụ, mật độ quang hoặc độ truyền qua dưới dạng hàm của bước sóng. Tuy nhiên, thông tin thường được trình bày dưới dạng đồ thị độ hấp thụ trên trục y thẳng đứng và bước sóng trên trục x nằm ngang. Biểu đồ này thường được gọi là phổ hấp thụ; một ví dụ được hiển thị trong Hình 4.
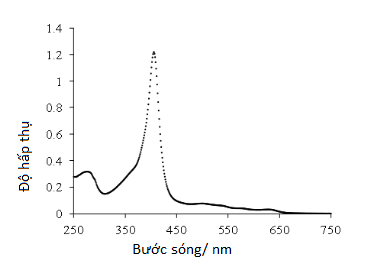
Hình 4: Một ví dụ về phổ hấp thụ được lấy từ máy quang phổ UV-Vis. Mẫu được kiểm tra là hemoglobin đã hết hạn được hòa tan trong dung dịch đệm phosphat có pH trung tính. Nhà cung cấp hình ảnh: Tiến sĩ Justin Tom.
Dựa trên thiết bị đo quang phổ UV ‑ Vis đã được xem xét trong phần trước của bài viết này, cường độ ánh sáng có thể được dự kiến một cách hợp lý có liên quan về mặt định lượng với lượng ánh sáng được mẫu hấp thụ.
Độ hấp thụ ( A ) bằng logarit của một phần liên quan đến cường độ ánh sáng trước khi truyền qua mẫu ( I o ) chia cho cường độ ánh sáng sau khi truyền qua mẫu ( I ). Phần tôi chia cho I o còn được gọi là độ truyền qua ( T ), biểu thị lượng ánh sáng đã truyền qua một mẫu. Tuy nhiên, định luật Beer – Lambert thường được áp dụng để thu được nồng độ của mẫu ( c ) sau khi đo độ hấp thụ ( A ) khi biết độ hấp thụ mol ( ε ) và chiều dài đường dẫn ( L ). Điển hình là εđược biểu thị với đơn vị là L mol ‑1 cm ‑1 , L có đơn vị là cm, và c được biểu thị với đơn vị là mol L ‑1 . Hệ quả là A không có đơn vị.
Đôi khi AU được sử dụng để chỉ các đơn vị tùy ý hoặc đơn vị hấp thụ nhưng điều này đã được khuyến khích mạnh mẽ.
Định luật Beer – Lambert đặc biệt hữu ích để thu được nồng độ của một chất nếu tồn tại mối quan hệ tuyến tính bằng cách sử dụng một tập hợp các dung dịch chuẩn được đo có chứa cùng một chất. Phương trình 1 cho thấy các mối quan hệ toán học giữa độ hấp thụ, định luật Beer-Lambert, cường độ ánh sáng đo được trong thiết bị và độ truyền qua.
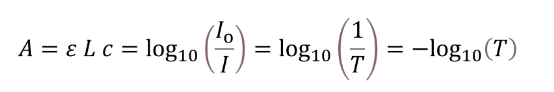 Phương trình 1: Một tập hợp các phương trình thể hiện mối quan hệ giữa độ hấp thụ A , định luật Beer – Lambert, cường độ ánh sáng đo được trong thiết bị và độ truyền qua.
Phương trình 1: Một tập hợp các phương trình thể hiện mối quan hệ giữa độ hấp thụ A , định luật Beer – Lambert, cường độ ánh sáng đo được trong thiết bị và độ truyền qua.
Thuật ngữ mật độ quang học (OD) đôi khi được sử dụng không chính xác để thay thế cho độ hấp thụ. OD và độ hấp thụ đều đo lượng cường độ ánh sáng bị mất trong một thành phần quang học, nhưng OD tính đến sự mất mát do tán xạ ánh sáng trong khi độ hấp thụ thì không. Nếu có rất ít tán xạ ánh sáng trong phép đo, thì OD có thể được tính gần đúng trực tiếp bằng cách sử dụng độ hấp thụ và có thể sử dụng định luật Beer – Lambert.
Biết các điều kiện thí nghiệm trong quá trình đo là quan trọng. Cuvet được thiết kế với chiều dài đường dẫn 1 cm là tiêu chuẩn và phổ biến nhất. Đôi khi, rất ít mẫu có sẵn để kiểm tra và độ dài đường dẫn ngắn hơn, nhỏ nhất là 1 mm là cần thiết. Khi cần định lượng, các giá trị độ hấp thụ phải được giữ dưới 1, trong dải động của thiết bị. Điều này là do độ hấp thụ bằng 1 ngụ ý rằng mẫu hấp thụ 90% ánh sáng tới, hoặc được phát biểu một cách tương đương là 10% ánh sáng tới được truyền qua mẫu. Với ít ánh sáng chiếu tới máy dò, một số máy quang phổ UV ‑ Vis không đủ nhạy để định lượng lượng ánh sáng một cách đáng tin cậy. Hai giải pháp đơn giản có thể thực hiện được cho vấn đề này là pha loãng mẫu hoặc giảm chiều dài đường dẫn.
Như đã đề cập ở trên, việc ghi lại phổ nền bằng dung dịch đối chiếu “trắng” là điều cần thiết. Nếu thiết bị hoàn hảo về mọi mặt, thì đường cơ sở sẽ không có độ hấp thụ đối với mọi bước sóng được kiểm tra. Tuy nhiên, trong tình huống thực tế, phổ nền thường sẽ có một số giá trị độ hấp thụ âm và dương rất nhỏ. Để thực hành tốt nhất, các giá trị độ hấp thụ nhỏ này thường được phần mềm tự động trừ đi các giá trị độ hấp thụ mẫu cho mỗi bước sóng ánh sáng để có được giá trị độ hấp thụ thực. 1
Tùy thuộc vào mục đích phân tích, việc xây dựng đường chuẩn có thể được mong muốn. Việc xây dựng đường chuẩn đòi hỏi một số phân tích dữ liệu và công việc bổ sung nhưng rất hữu ích để xác định chính xác nồng độ của một chất cụ thể trong mẫu dựa trên các phép đo độ hấp thụ. Tuy nhiên, có nhiều trường hợp không cần thiết phải sử dụng đường chuẩn bao gồm các phép đo OD để nuôi cấy vi khuẩn, lấy tỷ lệ độ hấp thụ ở các bước sóng cụ thể để đánh giá độ tinh khiết của axit nucleic hoặc xác định một số loại dược phẩm.
Trong quang phổ UV-Vis, bước sóng tương ứng với độ hấp thụ cực đại của chất đích được chọn để phân tích. Sự lựa chọn này đảm bảo độ nhạy tối đa vì đáp ứng lớn nhất thu được đối với một nồng độ chất phân tích nhất định. 1Ví dụ về phổ hấp thụ UV Vis của Food Green 3 và đường chuẩn tương ứng sử dụng các dung dịch chuẩn được đưa ra trong Hình 5. Lưu ý rằng hai đỉnh hấp thụ cực đại có trong thuốc nhuộm Food Green 3, một đỉnh hấp thụ cực đại nhỏ hơn ở 435 nm và cực đại hấp thụ cực đại mạnh hơn ở bước sóng 619 nm. Để đạt được độ nhạy tối đa khi tính toán nồng độ chưa biết của Food Green 3, đỉnh độ hấp thụ cực đại ở bước sóng 619 nm đã được sử dụng để phân tích. Các dung dịch chuẩn với một loạt các nồng độ đã biết được chuẩn bị bằng cách pha loãng dung dịch gốc, thực hiện các phép đo độ hấp thụ và sau đó vẽ các phép đo này trên biểu đồ độ hấp thụ so với nồng độ để xây dựng mối quan hệ bằng số giữa nồng độ và độ hấp thụ. Một đường chuẩn được tạo bằng phương trình hồi quy tuyến tính bình phương nhỏ nhất. Các điểm dữ liệu càng gần một đường thẳng thì càng phù hợp. Hệ số chặn y trong phương trình đường thẳng được đặt thành 0 để biểu thị không có độ hấp thụ khi không có thuốc nhuộm. Phương trình thể hiện trong Hình 5 được sử dụng để tính toán nồng độ của Food Green 3 (biến x) trong một mẫu chưa biết dựa trên độ hấp thụ đo được (biến y).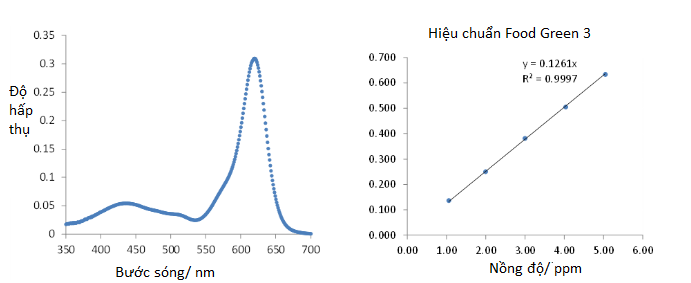 Hình 5: Phổ UV-Vis của Food Green 3 được chiết xuất từ một mẫu được hiển thị trên đồ thị bên trái. Đường chuẩn hiển thị trên đồ thị bên phải được phát triển từ các dung dịch pha loãng tiêu chuẩn của Food Green 3 sử dụng phương trình hồi quy tuyến tính bình phương nhỏ nhất. Nhà cung cấp hình ảnh: Tiến sĩ Justin Tom.
Hình 5: Phổ UV-Vis của Food Green 3 được chiết xuất từ một mẫu được hiển thị trên đồ thị bên trái. Đường chuẩn hiển thị trên đồ thị bên phải được phát triển từ các dung dịch pha loãng tiêu chuẩn của Food Green 3 sử dụng phương trình hồi quy tuyến tính bình phương nhỏ nhất. Nhà cung cấp hình ảnh: Tiến sĩ Justin Tom.
Đối với phân tích dữ liệu, biểu đồ của độ hấp thụ so với nồng độ có thể cho biết mức độ nhạy của hệ thống khi xây dựng đường chuẩn. Khi sử dụng phương trình hồi quy bình phương nhỏ nhất tuyến tính, độ dốc từ đường phù hợp nhất cho thấy độ nhạy. Nếu càng dốc thì độ nhạy càng cao. Độ nhạy là khả năng phân biệt sự khác biệt nhỏ về nồng độ mẫu. Từ Định luật Beer – Lambert, độ nhạy có thể được chỉ ra một phần bằng độ hấp thụ mol ε . Biết trước các giá trị ε , nếu có, có thể giúp xác định nồng độ của các mẫu cần thiết, đặc biệt ở những nơi có số lượng mẫu hạn chế hoặc đắt tiền.
Để có độ tin cậy và thực tiễn tốt nhất, nên lặp lại các thí nghiệm và phép đọc quang phổ UV ‑ Vis. Nói chung, khi lặp lại việc kiểm tra một mẫu, tối thiểu là ba lần thử nghiệm lặp lại, nhưng cần nhiều lần lặp lại nữa trong một số lĩnh vực công việc nhất định. Một đại lượng được tính toán, chẳng hạn như nồng độ của một mẫu chưa biết, thường được báo cáo là giá trị trung bình với độ lệch chuẩn. Các kết quả tái lập là điều cần thiết để đảm bảo các phép đo chính xác, chất lượng cao. Độ lệch chuẩn, độ lệch chuẩn tương đối hoặc hệ số biến thiên giúp xác định mức độ chính xác của hệ thống và các phép đo. Độ lệch hoặc độ biến thiên thấp cho thấy mức độ chính xác và độ tin cậy cao hơn.
Điểm mạnh và hạn chế của quang phổ UV-Vis
Không có kỹ thuật nào là hoàn hảo và quang phổ UV ‑ Vis cũng không ngoại lệ. Tuy nhiên, kỹ thuật này có một số điểm mạnh chính được liệt kê dưới đây khiến nó trở nên phổ biến.
- Kỹ thuật này không phá hủy, cho phép sử dụng lại mẫu hoặc tiếp tục xử lý hoặc phân tích thêm.
- Các phép đo có thể được thực hiện nhanh chóng , cho phép dễ dàng tích hợp vào các giao thức thử nghiệm.
- Các công cụ rất dễ sử dụng , yêu cầu người dùng ít đào tạo trước khi sử dụng.
- Phân tích dữ liệu thường yêu cầu xử lý tối thiểu , một lần nữa có nghĩa là cần ít đào tạo người dùng.
- Thiết bị này thường không đắt để mua và vận hành, giúp nhiều phòng thí nghiệm có thể sử dụng được.
Mặc dù điểm mạnh của kỹ thuật này có vẻ áp đảo, nhưng cũng có một số điểm yếu nhất định:
- Ánh sáng lạc hướng – Trong một thiết bị thực, các bộ chọn bước sóng không hoàn hảo và một lượng nhỏ ánh sáng từ dải bước sóng rộng vẫn có thể được truyền từ nguồn sáng, có thể gây ra sai số đo nghiêm trọng. Ánh sáng lạc cũng có thể đến từ môi trường hoặc ngăn được lắp lỏng lẻo trong thiết bị.
- Tán xạ ánh sáng – Tán xạ ánh sáng thường do chất rắn lơ lửng trong mẫu chất lỏng gây ra, có thể gây ra sai số đo nghiêm trọng. Sự hiện diện của bong bóng trong cuvet hoặc mẫu sẽ làm tán xạ ánh sáng, dẫn đến kết quả không thể thu được.
- Sự giao thoa từ nhiều loài hấp thụ – Ví dụ, một mẫu có thể có nhiều loại diệp lục sắc tố xanh lục. Các chất diệp lục khác nhau sẽ có phổ chồng lên nhau khi được kiểm tra cùng nhau trong cùng một mẫu. Để phân tích định lượng thích hợp, từng loại hóa chất cần được tách ra khỏi mẫu và kiểm tra riêng lẻ.
- Cân nhắc về mặt hình học – Vị trí không chính xác của bất kỳ bộ phận nào của thiết bị, đặc biệt là cuvet giữ mẫu, có thể mang lại kết quả không chính xác và không chính xác. Do đó, điều quan trọng là mọi thành phần trong thiết bị phải được căn chỉnh theo cùng một hướng và được đặt ở cùng một vị trí cho mọi phép đo. Do đó, một số đào tạo người dùng cơ bản thường được khuyến nghị để tránh sử dụng sai.
Các ứng dụng của quang phổ UV-Vis
UV ‑ Vis đã được ứng dụng vào nhiều mục đích và tình huống, bao gồm nhưng không giới hạn ở:
Phân tích DNA và RNA
Nhanh chóng xác minh độ tinh khiết và nồng độ của RNA và DNA là một trong những ứng dụng đặc biệt rộng rãi. Bản tóm tắt về các bước sóng được sử dụng trong phân tích của chúng và những gì chúng chỉ ra được đưa ra trong Bảng 1. Khi chuẩn bị các mẫu DNA hoặc RNA, ví dụ cho các ứng dụng cuối cùng như giải trình tự, điều quan trọng là phải xác minh rằng không có sự nhiễm bẩn nào với khác, hoặc với protein hoặc hóa chất được chuyển từ quá trình phân lập.
Tỷ lệ độ hấp thụ 260 nm / 280 nm (260/280) rất hữu ích để tiết lộ khả năng nhiễm bẩn trong các mẫu axit nucleic, được tóm tắt trong Bảng 2. DNA tinh khiết thường có tỷ lệ 260/280 là 1,8, trong khi tỷ lệ đối với RNA tinh khiết thường là 2,0 . DNA tinh khiết có tỷ lệ 260/280 thấp hơn RNA vì thymine, được thay thế bằng uracil trong RNA, có tỷ lệ 260/280 thấp hơn uracil. Các mẫu bị nhiễm protein sẽ giảm tỷ lệ 260/280 do độ hấp thụ cao hơn ở bước sóng 280 nm.
Bước sóng được sử dụng trong phân tích độ hấp thụ tính bằng nanomet | Sự hấp thụ tia cực tím ở bước sóng này cho thấy sự hiện diện của cái gì? | Nguyên nhân nào gây ra hiện tượng hấp thụ tia cực tím ở bước sóng này? |
| 230 | Chất đạm | Hình dạng protein |
| 260 | DNA và RNA | Adenine, guanine, cytosine, thymine, uracil |
| 280 | Chất đạm | Chủ yếu là tryptophan và tyrosine |
Bảng 1: Tóm tắt độ hấp thụ UV hữu ích khi xác định tỷ lệ độ hấp thụ 260/280 và 260/230.
| Tỷ lệ hấp thụ | Giá trị điển hình |
| 260/280 | 1,8 tỷ lệ độ hấp thụ đặc trưng cho DNA tinh khiết Tỷ lệ hấp thụ 2.0 điển hình cho RNA tinh khiết |
| 260/230 | Tỷ lệ hấp thụ thay đổi; 2,15 đến 2,50 điển hình cho RNA và DNA |
Bảng 2: Tóm tắt tỷ lệ hấp thụ UV dự kiến cho phân tích DNA và RNA.
Tỷ lệ độ hấp thụ 260 nm / 230 nm (260/230) cũng hữu ích để kiểm tra độ tinh khiết của các mẫu DNA và RNA và có thể tiết lộ sự nhiễm bẩn của protein hoặc hóa chất. Protein có thể hấp thụ ánh sáng ở bước sóng 230 nm, do đó làm giảm tỷ lệ 260/230 và cho thấy sự ô nhiễm protein trong các mẫu DNA và RNA. Guanidinium thiocyanat và guanidinium isothiocyanate, hai trong số các hợp chất phổ biến được sử dụng để tinh chế axit nucleic, hấp thụ mạnh ở bước sóng 230 nm, điều này cũng sẽ làm giảm tỷ lệ hấp thụ 260/230.
Phân tích dược phẩm
Một trong những ứng dụng phổ biến nhất của quang phổ UV-Vis là trong ngành dược phẩm. Đặc biệt, xử lý phổ UV-Vis bằng cách sử dụng các dẫn xuất toán học cho phép phân giải các đỉnh hấp thụ chồng lên nhau trong phổ gốc để xác định các hợp chất dược phẩm riêng lẻ. Ví dụ, benzocaine, chất gây tê cục bộ và chlortetracycline, một loại kháng sinh, có thể được xác định đồng thời trong các công thức bột thú y thương mại bằng cách áp dụng dẫn xuất toán học đầu tiên cho phổ độ hấp thụ. Có thể định lượng đồng thời cả hai chất trên dải nồng độ microgam trên mililit bằng cách xây dựng hàm hiệu chuẩn cho từng hợp chất.
Nuôi cấy vi khuẩn
Quang phổ UV-Vis thường được sử dụng trong nuôi cấy vi khuẩn . Các phép đo OD được thực hiện thường xuyên và nhanh chóng bằng cách sử dụng bước sóng 600 nm để ước tính nồng độ tế bào và theo dõi sự phát triển. 600 nm thường được sử dụng và ưa thích do các đặc tính quang học của môi trường nuôi cấy vi khuẩn trong đó chúng được nuôi cấy và để tránh làm hỏng tế bào trong những trường hợp cần phải tiếp tục thử nghiệm.
Phân tích đồ uống
Việc xác định các hợp chất cụ thể trong đồ uống là một ứng dụng phổ biến khác của quang phổ UV-Vis. Hàm lượng caffein phải nằm trong giới hạn pháp lý nhất định, mà ánh sáng tia cực tím có thể tạo điều kiện cho việc định lượng. Một số loại chất màu nhất định, chẳng hạn như anthocyanin có trong quả việt quất, mâm xôi, mâm xôi và anh đào, có thể dễ dàng xác định bằng cách khớp với bước sóng hấp thụ đỉnh đã biết của chúng trong rượu vang để kiểm soát chất lượng bằng cách sử dụng độ hấp thụ UV-Vis.
Các ứng dụng khác
Kỹ thuật này cũng có thể được sử dụng trong nhiều ngành công nghiệp khác. Ví dụ, đo chỉ số màu rất hữu ích để theo dõi dầu máy biến áp như một biện pháp phòng ngừa để đảm bảo nguồn điện được cung cấp một cách an toàn. Đo độ hấp thụ của hemoglobin để xác định nồng độ hemoglobin có thể được sử dụng trong nghiên cứu ung thư. Trong xử lý nước thải, quang phổ UV-Vis có thể được sử dụng trong các nghiên cứu động học và giám sát để đảm bảo một số thuốc nhuộm hoặc sản phẩm nhuộm đã được loại bỏ đúng cách bằng cách so sánh phổ của chúng theo thời gian. Nó cũng tìm thấy tiện ích tuyệt vời trong việc phân tích tính xác thực của thực phẩm và giám sát chất lượng không khí .
Quang phổ UV ‑ Vis cũng hữu ích về mặt chất lượng trong một số nghiên cứu chuyên biệt hơn. Theo dõi các thay đổi trong bước sóng tương ứng với độ hấp thụ đỉnh rất hữu ích trong việc kiểm tra các thay đổi cấu trúc cụ thể của protein và trong việc xác định thành phần pin. Sự thay đổi bước sóng độ hấp thụ đỉnh cũng có thể hữu ích trong các ứng dụng hiện đại hơn như xác định đặc tính của các hạt nano rất nhỏ. Các ứng dụng của kỹ thuật này rất đa dạng và dường như vô tận.
